ЭНЕРГИИ СВЯЗЕЙ ЗАМЕЩЕННЫХ МЕТАНА И ЕГО АНАЛОГОВ
Наличие надежных расчетных методов позволяет предсказывать хаpaктеристики вещества и выбрать те соединения, которые (согласно прогнозу) удовлетворяют поставленным требованиям. Это закладывает научные основы создания новых веществ и материалов с заранее заданными свойствами.
Нами проведен анализ экспериментальных (и расчетных) данных по энергиям связей в ряде замещенных метана и его аналогов по подгруппе- силана, моногермана, станнана и т.д. вида ЭН4-lXl, ЭН4-l-mXlYm,... (Э = С, Si, Ge, Sn, Pb; X,Y,... = D, T, F,..., СН3, ...). Проведена систематизация средних энергий связей и энергий разрыва связей в этих соединениях. Выявлены определенные закономерности, выполнены численные расчеты.
Энергия связи (термохимическая) e - это доля энтальпии атомизации (DаН0) молекулы, приходящаяся на данную связь в этой молекуле (так, что сумма по всем энергиям связей равна DаН0). Для молекул вида ЭХn (с одинаковыми связями) средняя энергия связи вычисляется по формуле
eэ-х = (1/n)DаН0эхn = (1/n)[DfН0э + nDfН0x -DfН0эхn]
(DfН0 - энтальпия образования из элементов).
Энергия разрыва связи (D) определяется как тепловой эффект реакции гомолитического (или гетеролитического) распада по данной связи. Средняя энергия С-Н связи в молекуле метане связана с энергиями разрыва связей соотношением
eс0-н = (1/4)(Dсн3-н + Dсн2-н + Dсн-н + Dс-н).
При учёте попарных взаимодействий энергии разрыва связей в ряду СН4-lХl можно записать как квадратичную функцию степени замещения l [2]
- Dcl-н = d0 +d1l+d2l2 (l = 0, 1, 2, 3),
- Dcl-х = ď0 +ď1l+ď2l2 (l = 1, 2, 3, 4),
где d0, d1, d2, ď0, ď1, ď2 - параметры, выражающиеся через валентные и невалентные взаимодействия.
Если выполняется постулат о среднем арифметическом для невалентных взаимодействий, а именно: взаимодействия разнородных частиц (например, НХ) равно полусумме взаимодействий однородных (например, НН и ХХ), то энергии разрыва связей становятся линейными функциями l.
При учете тройных взаимодействий невалентных атомов, энергии связей будут кубическими функциями l.
Подобные соотношения имеют место для энергий гетеролитического разрыва связей [2].
Анализ экспериментальных числовых данных по eс-х (при 298 К) и D298 (см. [3]) позволяет выявить определенные закономерности:
1. Влияние изотопного замещения на энергии связей мало; оно в ряду СН4, СD4, СT4 несколько повышает величину eс-х. Ср. eс-х (в кДж/моль):
CH4 (415,8) СD4 (423,6) СT4 (426,8)
2. Энергии связей eс-х в гидридах СН4, SiH4, GeH4, SnH4, PbH4 монотонно уменьшаются с увеличением атомного номера. Ср. eс-х (в кДж/моль):
СН4, (415,8) SiH4 (322,2) GeH4 (289,5) SnH4 (252,7) PbH4 (199,8)
3. Энергии связей eс-х в ряду СН4, СF4, СCl4, СBr4, СI4 изменяются немонотонно (сначала увеличиваются, достигая максимума в тетрафториде углерода, затем уменьшаются). Ср. eс-х (в кДж/моль):
СН4, (415,8) CF4 (492,1) CCl4 (324,4) CBr4 (262,0) CI4 (189,0)
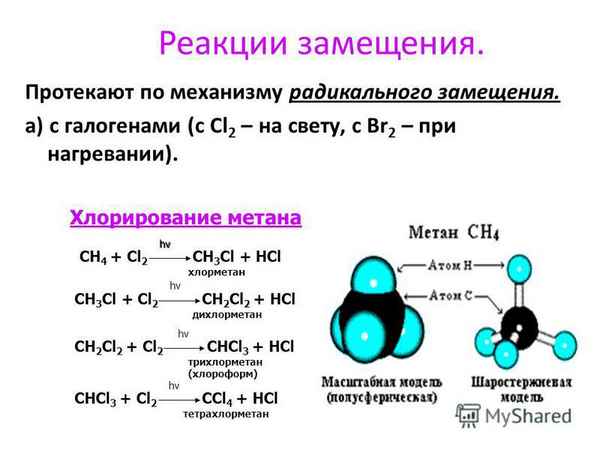
4. Величины D298 обычно уменьшаются с ростом степени замещения. Это уменьшение, как правило, происходит монотонно, в частности, линейно. Ср. D298 (в Дж/моль) для хлорзамещенных метана:
CH3-Cl CH2Cl -Cl CHCl2-Cl CCl3-Cl
350 339±13 323±21 307±8
CH3-H CH2Cl-H CHCl2-H CCl3-H
435±4 426±13 415 402±13
5. Есть случаи, где величины D298, вероятно, увеличиваются с ростом степени замещения. Ср. D298 (в кДж/моль) для фторзамещенных метана:
CH3-F CH2F-F CHF2-F CF3-F
469 479±21 536±21 540±13
CH3-H CH2F-H CHF2-H CF3-H
435±4 419 421±21 444±4
6. В целом ряде случаев величины D298 изменяются немонотонно или же мало меняются с накоплением заместителей (в кДж/моль):
CH3-X CH2X-X CHX2-X CX3-X
X = I 234±4 218 230 185
CH3-H CH2X-H CHX2-H CX3-H
X = I 435±4 434±8 431 393
7. В ряде случаев D298 слабо зависят от строения алкильной группы. Сюда попадают алканолы R-ОН, тиолы R-SH, амины R-NН2 (кДж/моль):
CH3-X CH3CH2-X (CH3)2CH-X (CH3)3C-X
X = OH 383±4 381±4 389±13 388
X = SH 311±4 300±9 295 292
X = NH2 338±14 336±10 334 336
Работа выполнена при финансовой поддержке Российского фонда фундамен-тальных исследований (проект 04-03-96703р2004Центр-а)
СПИСОК ЛИТЕРАТУРЫ
- Папулов Ю.Г, Левин В.П., Виноградова М.Г. Строение вещества в естественнонаучной картине мира: Молекулярные аспекты. Учебное пособие, 2-ое издание. Тверь: ТвГУ, 2005. 208 с.
- Ю.Г. Папулов, М.Г. Виноградова. Расчетные методы в атом-атомном представлении: Монография. Тверь: ТвГУ, 2002. 232 с.
- Папулов Ю.Г., Виноградова М.Г. Феноменологические методы исследования взаимосвязи «структура - свойство» в атом-атомном представлении //Вестн. Твер. гос. ун-та. Сер. Химия. 2005. № 2. С. 5-40.
 На основе введённых функций состояния для электромагнитного поля и зарядовой функции состояния для частиц выведена полная система уравнений Максвелла для электродинамики. Показано, что закон сохранения зарядов есть следствие существования этой функции. Показано также, что в вакууме электромагнитное поле отсутствует, что подтверждает справедливость теории дальнодействия.
...
На основе введённых функций состояния для электромагнитного поля и зарядовой функции состояния для частиц выведена полная система уравнений Максвелла для электродинамики. Показано, что закон сохранения зарядов есть следствие существования этой функции. Показано также, что в вакууме электромагнитное поле отсутствует, что подтверждает справедливость теории дальнодействия.
...
01 05 2024 4:21:36
 Статья в формате PDF
263 KB...
Статья в формате PDF
263 KB...
30 04 2024 15:32:58
 Статья в формате PDF
233 KB...
Статья в формате PDF
233 KB...
29 04 2024 16:59:21
 В статье исследованы некоторые проблемы опережающего антикризисного управления предприятием.
...
В статье исследованы некоторые проблемы опережающего антикризисного управления предприятием.
...
28 04 2024 17:18:15
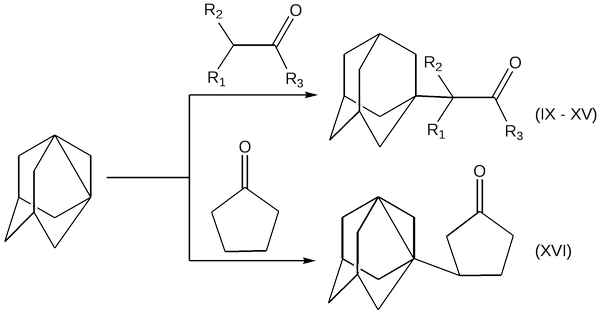 В статье рассмотрены реакции 1,3-дегидроадамантана, относящегося к напряженным мостиковым [3.3.1]пропелланам, с диметилтрисульфидом. Установлено, что при взаимодействии образуются 1,3-бис(метилтио)адамантан, 1-(метилдитио)-3-(метилтио)адамантан и 1,3-бис(метилдитио)адамантан в соотношении 1:4,5:1. Структуры полученных соединений подтверждены методами хромато-масс-спектометрии и ЯМР1Н-спектроскопии. Выход целевого 1-(метилдитио)-3-(метилтио)адамантана составляет 50 %. Было предположено, что реакция протекает по радикальному механизму. Приведено описание эксперимента.
...
В статье рассмотрены реакции 1,3-дегидроадамантана, относящегося к напряженным мостиковым [3.3.1]пропелланам, с диметилтрисульфидом. Установлено, что при взаимодействии образуются 1,3-бис(метилтио)адамантан, 1-(метилдитио)-3-(метилтио)адамантан и 1,3-бис(метилдитио)адамантан в соотношении 1:4,5:1. Структуры полученных соединений подтверждены методами хромато-масс-спектометрии и ЯМР1Н-спектроскопии. Выход целевого 1-(метилдитио)-3-(метилтио)адамантана составляет 50 %. Было предположено, что реакция протекает по радикальному механизму. Приведено описание эксперимента.
...
27 04 2024 14:52:35
 Статья в формате PDF
175 KB...
Статья в формате PDF
175 KB...
26 04 2024 11:44:41
 Статья в формате PDF
121 KB...
Статья в формате PDF
121 KB...
25 04 2024 17:29:30
 Статья в формате PDF
264 KB...
Статья в формате PDF
264 KB...
23 04 2024 5:44:42
 Статья в формате PDF
106 KB...
Статья в формате PDF
106 KB...
22 04 2024 14:15:45
21 04 2024 23:31:12
 Статья в формате PDF
136 KB...
Статья в формате PDF
136 KB...
19 04 2024 4:39:46
 Статья в формате PDF
111 KB...
Статья в формате PDF
111 KB...
18 04 2024 4:37:35
 Статья в формате PDF
140 KB...
Статья в формате PDF
140 KB...
17 04 2024 2:29:29
 Статья в формате PDF
115 KB...
Статья в формате PDF
115 KB...
16 04 2024 4:50:34
 Статья в формате PDF
119 KB...
Статья в формате PDF
119 KB...
15 04 2024 7:32:29
 Статья в формате PDF
109 KB...
Статья в формате PDF
109 KB...
14 04 2024 15:39:41
 Статья в формате PDF
113 KB...
Статья в формате PDF
113 KB...
12 04 2024 4:59:32
 Статья в формате PDF
133 KB...
Статья в формате PDF
133 KB...
11 04 2024 20:43:17
 Статья в формате PDF
118 KB...
Статья в формате PDF
118 KB...
10 04 2024 3:45:10
 Статья в формате PDF
125 KB...
Статья в формате PDF
125 KB...
08 04 2024 13:38:59
 Статья в формате PDF
116 KB...
Статья в формате PDF
116 KB...
07 04 2024 20:21:47
 Статья в формате PDF
262 KB...
Статья в формате PDF
262 KB...
06 04 2024 14:13:52
 Статья в формате PDF
219 KB...
Статья в формате PDF
219 KB...
05 04 2024 18:43:55
 Рассмотрена концепция зависимости лесов как ядра биосферы Земли от активности Солнца по числу Вольфа. Принята точка на Земле в виде участка лесистой территории национального парка по лесным пожарам за 2002 год. По датам каждого лесного пожара были учтены: время от зимнего солнцестояния с 21 марта, склонение оси Земли к Солнцу, число Вольфа активности Солнца на день возникновения лесного пожара. Среди влияющих факторов первое место заняло время от зимнего солнцестояния. Второе место – склонение Солнца, а на третье – число Вольфа. Среди зависимых факторов первым стало склонение Солнца, вторым – время от 21.03, а третьим активность Солнца. В итоге параметры Земли первичны. Наиболее опасен интервал числа Вольфа 90 ≤ V ≤ 180 и сильный размах колебания во многом зависит от поведения людей.
...
Рассмотрена концепция зависимости лесов как ядра биосферы Земли от активности Солнца по числу Вольфа. Принята точка на Земле в виде участка лесистой территории национального парка по лесным пожарам за 2002 год. По датам каждого лесного пожара были учтены: время от зимнего солнцестояния с 21 марта, склонение оси Земли к Солнцу, число Вольфа активности Солнца на день возникновения лесного пожара. Среди влияющих факторов первое место заняло время от зимнего солнцестояния. Второе место – склонение Солнца, а на третье – число Вольфа. Среди зависимых факторов первым стало склонение Солнца, вторым – время от 21.03, а третьим активность Солнца. В итоге параметры Земли первичны. Наиболее опасен интервал числа Вольфа 90 ≤ V ≤ 180 и сильный размах колебания во многом зависит от поведения людей.
...
04 04 2024 8:35:32
 Статья в формате PDF
118 KB...
Статья в формате PDF
118 KB...
03 04 2024 2:19:44
 Статья в формате PDF
128 KB...
Статья в формате PDF
128 KB...
02 04 2024 20:51:20
 Статья в формате PDF
165 KB...
Статья в формате PDF
165 KB...
01 04 2024 1:27:57
 Статья в формате PDF
121 KB...
Статья в формате PDF
121 KB...
31 03 2024 14:11:42
 Статья в формате PDF
122 KB...
Статья в формате PDF
122 KB...
30 03 2024 22:21:55
 Статья в формате PDF
152 KB...
Статья в формате PDF
152 KB...
29 03 2024 18:20:29
 Статья в формате PDF
115 KB...
Статья в формате PDF
115 KB...
28 03 2024 4:31:53
 Статья в формате PDF
364 KB...
Статья в формате PDF
364 KB...
27 03 2024 11:55:30
 Статья в формате PDF
325 KB...
Статья в формате PDF
325 KB...
26 03 2024 15:44:42
 Статья в формате PDF
100 KB...
Статья в формате PDF
100 KB...
25 03 2024 3:55:10
 Статья в формате PDF
111 KB...
Статья в формате PDF
111 KB...
24 03 2024 10:24:55
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::