БИОХИМИЧЕСКИЕ И ТОКСИКОЛОГИЧЕСКИЕ ОСОБЕННОСТИ МИКОТОКСИНОВ, ПРОДУЦИРУЕМЫХ ГРИБАМИ-ПАТОГЕНАМИ ОЗИМОЙ ПШЕНИЦЫ

МТ - это вторичные метаболиты микроскопических грибов, обладающие выраженными токсическими свойствами, т.е. метаболиты, не являющиеся эссенциальными для роста и развития продуцирующих их микроорганизмов [8]. МТ образуются из первичных метаболитов в результате изменения физиологических факторов, как, например, содержания питательных веществ, соотношения микроэлементов и других факторов роста. Усиленное образование МТ может, вероятно, быть свидетельством нарушения равновесия между микроскопическими грибами и окружающей средой. К настоящему времени достигнуты значительные успехи в установлении распространенности, химической структуры МТ, изучении их физико-химических свойств, разработке методов анализа. Менее изучены особенности биогенеза, метаболизма и механизмов действия. В.А.Тутельян полагает, что число известных МТ будет увеличиваться по мере изучения роли микроскопических грибов в развитии алиментарных токсикозов человека и животных с пока неясной этиологией [8].
МТ образуются в цепи последовательных ферментных реакций из относительно небольшого числа химически простых промежуточных продуктов основного метаболизма, таких как ацетат, малонат, мевалонат и аминокислоты [8]. Наиболее значимыми этапами биосинтеза МТ являются реакции конденсации, окисления-восстановления, алкилирования и галогенизации, которые приводят к образованию весьма различных по структуре предшественников МТ. Известно пять основных путей биосинтеза МТ [3, 8]: поликетидный, хаpaктерный для патулина (тетpaкетиды), охратоксина А (пентакетиды), мальторизина (гексакетиды), виомеллеина (гептакетиды), эргохромов (октакетиды), зеараленона (нонакетиды), афлатоксинов и стеригматоцистина (декакетиды) и др.; терпеноидный - для трихотеценовых МТ (ТТМТ); через цикл трикарбоновых кислот - для рубратоксинов; аминокислотный, в котором исходными соединениями являются аминокислоты-эргоалкалоиды, споридесмин, циклопиазоновая кислота и др.; смешанный (сочетание двух или более основных путей) - для производных циклопиазоновой кислоты. Наибольший интерес представ-ляет поликетидный путь - основной для биосинтеза большой группы МТ. В основе его лежит линейная конденсация ацетил-СоА с тремя или более молекулами малонил-СоА с сопутствующим декарбоксилированием, но без обязательного восстановления промежуточных β-дикарбонильных систем. Исходя из числа С2-единиц, включенных в молекулу, МТ, синтезирующиеся этим путем, подразделяются на тетра-, пента-, гекса-, гепта-, окта-, нона- и декакетиды. Терпеноидный путь биосинтеза, хаpaктерен для большой группы ТТМТ. Начинает цепь превращений мевалонат, важным этапом является продукция фарнезилпирофосфата; образование основной циклической системы трихотеценовой молекулы осуществляется циклизацией фарнезилпирофосфата - превращение в триходиен, триходиол и, наконец, 12,13-эпокситрихотецен. Последующие этерификация, гидроксилирование трихотеценового ядра приводят к синтезу триходермола, веррукарола, трихотеколона и трихотецина. Полагают, что биогенез трихотеценового ядра идентичен у всех видов Trichothecium и Fusarium, но синтез разных ТТМТ отличается особенностями в процессе гидроксилирования, катализируемом ферментными системами, генетически своеобразными у разных видов грибов.
Единая таксономия микроскопических грибов, классификация и номенклатура МТ в целом отсутствует [8]: в одних случаях в основу группового деления МТ положена их химическая структура, в других - хаpaктер токсического действия, в третьих - видовая принадлежность грибов-продуцентов.
Содержание МТ в зерне должно строго регламентироваться, так как они представляют серьезную опасность для здоровья человека и животных. Наиболее существенное значение в силу токсических свойств и повсеместного распространения традиционно придается афлатоксинам, охратоксинам, ТТМТ, эрготоксинам, зеараленону (ЗЛ) и патулину, хотя потенциально опасными для человека являются и другие токсины. Однако в последние годы внимание все большее переходит от афлатоксинов к ТТМТ [8].
Афлатоксины обладают широким спектром токсикологических эффектов [1, 3, 4, 8]: гепатотоксическим, канцерогенным, мутагенным, тератогенным, нейротоксическим, цитотоксическим, иммунодепрессивным; способны нарушать репродуктивные функции и эндокринный статус, провоцировать злокачественные опухоли печени, легких, кишечника; вызывали массовые cмepтельные отравления населения в Индии и Таиланде. Поступление с пищей 2 мг/кг токсина В1 влечет за собой летальный исход.
Охратоксикозы [5, 8] приводят к заболеваемости и cмepтности населения вследствие нефропатии, опухолей мочевыводящих путей и печени. Известны тератогенные, противосвертывающие, треморогенные, канцерогенные свойства охратоксинов. МТ грибов рода Aspergillus вызывают пять инвазивных и аллергических синдромов.
Патулин, продуцируемый грибами Penicillium), оказывает на организм через зараженные фрукты и овощи мутагенное, тератогенное, иммуномодулирующее и цитонекротическое действие [3, 4]. Отравления эрготоксинами (из склероциев спорыньи), связанные с мукой и хлебопродуктами, имеют гангренозные и судорожные формы [3].
ТТМТ составляют наиболее распространенную группу из более чем 40 метаболитов различных видов грибов Fusarium, Cephalosporium, Myrothecium и др. Тpaктовка данных о токсических свойствах рода Fusarium, полученных разными авторами в различных странах, осложнена отсутствием единой систематики этого рода [8]. Согласно классификации В.И.Билай [2], основные продуценты ТТМТ типа относятся к виду F.sporotrichiella, a F. tricinctum и F. poae являются его разновидностями, т.е. F. sporotrichiella var. tricinctum и F. sporotrichiella var poae. Кроме того, один и тот же вид гриба-продуцента в зависимости от условий культивирования может синтезировать несколько ТТМТ разных типов [3, 8]. Химическая структура ТТМТ относится к сесквитерпенам [7, 8]. Они содержат основное ядро из трех колец (трихотекан). Поскольку ТТМТ содержат эпоксидное кольцо при С-12 - С-13 и двойную связь при С-9 - С-10, вся группа получила название 12,13-эпокситрихотец-9-ены. В зависимости от структуры трихотеценового ядра они разделяются на 4 группы: тип А составляют соединения, содержащие при С-8 в качестве радикала Н, либо ОН (табл. 1); тип В - соединения, имеющие у С-8 карбоксильную группу (табл. 2); тип С - макроциклические ТТМТ; тип D включает соединения, содержащие второй эпоксид при С-7 - С-8.
Таблица 1. Структура трихотеценовых микотоксинов типа А
|
Микотоксин |
R1 |
R2 |
R3 |
R4 |
R5 |
|
Тип А |
|
||||
|
Триходермол |
H |
OH |
H |
H |
H |
|
Триходермин |
H |
OCOCH3 |
H |
H |
H |
|
Веррукарол |
H |
OH |
OH |
H |
H |
|
Скирпентриол |
OH |
OH |
OH |
H |
H |
|
Моноацетоксискирпенол |
OH |
OH |
OCOCH3 |
H |
H |
|
Диацетоксискирпенол |
OH |
OCOCH3 |
OCOCH3 |
H |
H |
|
7,8-Дигидроксиди-ацетоксискирпенол |
OH |
OCOCH3 |
OCOCH3 |
OH |
OH |
|
Т-2-Тетраол |
OH |
OH |
OH |
H |
OH |
|
Неосоланиол |
OH |
OCOCH3 |
OCOCH3 |
H |
OH |
|
НТ-2-Токсин |
OH |
OH |
OCOCH3 |
H |
OCOCH2CH(CH3)2 |
|
Т-2-Токсин |
OH |
OCOCH3 |
OCOCH3 |
H |
OCOCH2CH(CH3)2 |
|
Т-2-Триол |
OH |
OH |
OH |
H |
OCOCH2CH(CH3)2 |
Таблица 2. Структура трихотеценовых микотоксинов типа В
|
Микотоксин |
R1 |
R2 |
R3 |
R4 |
|
Тип В |
|
|||
|
Трихотеколон |
H |
OH |
H |
H |
|
Трихотецин |
H |
OCOCH=CHCH3 |
H |
H |
|
Ниваленол |
OH |
OH |
OH |
OH |
|
Дезоксиниваленол |
OH |
H |
OH |
OH |
|
Фузаренон-Х |
OH |
OCOCH3 |
OH |
OH |
|
Диацетилниваленол |
OH |
OCOCH3 |
OCOCH3 |
OH |
|
Тетраацетилниваленол |
OCOCH3 |
OCOCH3 |
OCOCH3 |
OCOCH3 |
В качестве природных контаминантов пищевых продуктов и кормов среди фузариотоксинов встречаются главным образом ниваленол, дезоксиниваленол (ДОН, вомитоксин), токсин Т-2 и диацетоксискирпенол (ДАС) [4], причем из них наибольшее значение придается ДОН и Т-2 токсину [7]. Имеются отдельные сообщения о выявлении в зерновых НТ-2-токсина, неосоланиола и биологического предшественника ДОН - 3-ацетилдезоксиниваленола (3-ацДОН) [8]. На токсинообразование влияет химический состав среды культивирования: максимальный синтез токсинов наблюдается при наличии в качестве источника углерода целлобиозы, галактозы, мальтозы, маннита и крахмала, а в качестве источника азота - мочевины, углекислого ацетата и цитрата аммония, а также некоторых аминокислот (аланина, глицина, аспарагина, валина, тирозина и глутаминовой кислоты). Избыток серы и железа стимулирует синтез МТ, дефицит серы - подавляет; цинк, ванадий и магний стимулируют, а кобальт полностью подавляет рост мицелия.
ТТМТ представляют собой бесцветные кристаллические, химически стабильные соединения, плохо растворимые в воде. МТ типа А растворимы в умеренно полярных растворителях (ацетон, этилацетат, хлороформ); типа В - в более полярных (этанол, метанол). В целом ТТМТ типа А более токсичны, чем В, а соединения типа D, несмотря на две эпоксидные группы, - малотоксичны. Восстановление двойной связи при С-9;10 приводит к незначительному снижению токсичности, в то время как размыкание эпоксидного кольца лишает МТ биологической активности. Эпоксид при С-12, С-13 очень стабилен и для размыкания этого кольца необходимы жесткие воздействия, например, концентрированными кислотами, перекисью водорода, длительным кипячением [8].
Эти токсины, за исключением лишь некоторых макроциклических, не обладают флюоресценцией, и для их обнаружения после разделения методом тонкослойной хроматографии (ТСХ) применяют различные способы обработки с целью получения окрашенных или флюоресцирующих производных. При обработке хроматограмм 10-50% спиртовым раствором Н2SO4 с последующим нагреванием при 100-150оС ТТМТ типа А приобретают серую или пурпурную окраску, а типа В - коричневую. МТ типа А после обработки кислотой флюоресцируют гoлyбым цветом в ультрафиолете (360 нм). Гoлyбая флюоресценция у токсинов типа В появляется после обработки хроматографических пластин 50% раствором хлорида алюминия и нагревания при 130оС. Эффективным хромогенным реагентом является n-анисовый альдегид, обработка которым хроматографических пластин с последующим нагреванием при 100-130оС приводит к образованию пурпурно-красных производных токсинов типа А и желтых - типа В. После обработки ТТМТ типа А приобретают способность флюоресцировать гoлyбым цветом в длинноволновой области ультрафиолета. В качестве хромогенного реагента для выявления всех типов ТТМТ, имеющих эпоксидную группу при С-12, С-13, возможно использование 4-(п-нитробензил)-пиридина, при обработке которым токсины приобретают сине-фиолетовую окраску [8]. Тем не менее, по-прежнему одной из причин малочисленности данных о распространенности ТТМТ является отсутствие высокочувствительных и достаточно простых и надежных методов их анализа.
Отравление ТТМТ хаpaктеризуется [3, 7, 8] поражением центральной нервной системы, желудочно-кишечного тpaкта, кожи, кровеносной, кроветворной, иммунной и других систем, тератогенным действием. Высокое содержание фузариотоксинов (токсин Т-2, ниваленол, ДОН, ДАС) в зерновке (и соломе) может быть причиной массовых отравлений.
Метаболизм Т-2 токсина осуществляется при участии микросомных ферментных систем [8]: он подвергается деацетилированию с образованием НТ-2 токсина, затем 4-деацетилнеосоланиола и, наконец, Т-2-тетраола. Таким образом, 4-деацетилнеосоланиол и Т-2-тетраол представляют собой продукты детоксикации Т-2 токсина в организме. Существует и другой путь биотрaнcформации Т-2 токсина: Т-2 токсин → неосоланиол → 4-деацетилнеосоланиол → Т-2-тетраол. Реакция С-4-деацетилирования катализируется микросомной неспецифической карбоксилэстеразой. Наряду с деацетилированием Т-2 токсин может подвергаться окислению с образованием оксипроизводных Т-2 и НТ-2 токсинов. Гидроксилирование последних происходит при участии цитохром Р-450-зависимых монооксигеназ.
Метаболизм (детоксикация) ДОН протекает в направлении образования деэпоксидированного производного - 3α,7α,15-тригидрокси-трихотец-9,12-диен-8-он. Остается неясным, способна ли микросомальная эпоксигидролаза участвовать в обезвреживании ТТМТ, а также значение реакций конъюгации с SH-глутатионом, UDP-глюкуроновой кислотой и другими соединениями, которые, как известно, играют существенную роль в детоксикации 2,3-эпоксида афлатоксина В1. Тем не менее, ряд косвенных признаков указывают на важную роль реакций конъюгации в детоксикации Т-2 токсина [8].
Грибы рода Fusarium наряду с ТТМТ способны продуцировать и другие МТ, например, зеараленон (ЗЛ) - лактон 6-(101-окси-61-оксо-трaнc-11-ундеценил)-β-резорциловой кислоты с эмпирической формулой С18Н22О5 и молекулярной массой 318. Это белое кристаллическое вещество с температурой плавления 164-165оС, с трaнc-конфигурацией, ограниченно растворимое в воде и хорошо растворимое в спиртах, ацетоне, хлороформе. ЗЛ обладает сине-зеленой флуоресценцией в ультрафиолетовом свете при 360 нм. [3, 8]. Основными продуцентами ЗЛ являются F. graminearum (F. roseum), F. moniliforme и F.tricinctum.
Известны его эстрогенные, мутагенные, тератогенные (эмбриотоксические) и канцерогенные свойства, склонность нарушать репродуктивную функцию и вызывать преждевременное пoлoвoе созревание [3, 8]. ЗЛ подвергается быстрой биотрaнcформации в организме. Около 60% его метаболитов представлены легко выводящимися малотоксичными конъюгатами (глюкуронидами), а 25% - α-зеараленолом, который в силу высокой эстрогенной активности рассматривают как активированную форму ЗЛ. В числе активных метаболитов ЗЛ известны α- и β-зеараленол, а также α- и β-зеараланол.
Особую значимость имеет проблема воздействия МТ на иммунную защиту организма, являясь одной из главных причин роста инфекционной, аутоиммунной, аллергической и oнкoлoгической заболеваемости. Она и потребует в будущем первоочередного решения.
Список литературы
- Афлатоксины. Сер.: Обзоры научной литературы по токсичности и опасности химических веществ / Под ред. Н.Ф.Измерова. - М., 1993. - С.26-27.
- Билай В.И.; Курбацкая З.А. Определитель токсинообразующих микромицетов. - Киев: Наукова думка, 1990. - 236 с.
- Донченко Л.В., Надыкта В.Д. Безопасность пищевой продукции. - М.: Пищепромиздат, 2001. - 528 с.
- Кравченко Л.В. Микотоксины как природные контаминанты пищевых продуктов и кормов //Оценка загрязнения пищевых продуктов микотоксинами. - М., 1985. - Т.2. - С.7-28.
- Кравченко Л.В., Авреньева Л.И., Тутельян В.А. Оценка комбинированного действия микотоксинов дезоксиниваленола (вомитоксина) и Т-2 токсина на крыс //Токсикологический вестник. - 2000. - №1. - C.2-8.
- Монастырский О.А. Современное состояние и проблемы исследования токсиногенных грибов, поражающих злаковые культуры //Актуальные вопросы биологизации защиты растений. - Пущино, 2000. - С.79-89.
- Соболев В.С. Химические методы анализа трихотеценовых микотоксинов. Краткие сведения о трихотеценах //Оценка загрязнения пищевых продуктов микотоксинами. - М., 1985. - Т.3. - С.216-239.
- Тутельян В.А., Кравченко Л.В. Микотоксины (медицинские и биологические аспекты). - М.: Медицина, 1985. - 320 с.
Работа представлена III научную конференцию с международным участием «Медицинские, социальные и экономические проблемы сохранения здоровья населения», г. Анталия (Турция), 22-29 мая 2005 г. Поступила в редакцию 11.04.2005 г.
 Статья в формате PDF
103 KB...
Статья в формате PDF
103 KB...
02 05 2024 8:13:33
 Статья в формате PDF
274 KB...
Статья в формате PDF
274 KB...
01 05 2024 16:49:46
 Статья в формате PDF
257 KB...
Статья в формате PDF
257 KB...
30 04 2024 12:33:56
 Статья в формате PDF
118 KB...
Статья в формате PDF
118 KB...
28 04 2024 4:41:35
 Понятие время является важнейшим понятием, как физики, так и философии. Актуальность этой проблемы обусловлена тем, что до сих пор, несмотря на широкий круг исследований, не сложилось твердо закрепленного представления о времени. В статье делается попытка раскрыть сущность понятия времени и связать меру времени с движением. За меру времени механического движения предлагается выбрать путь, пройденный, например, концом стрелки часов, участвующей не только в собственном движении относительно циферблата, как это принято, но и в сложном движении, включающем движение часов как целое относительно внешнего наблюдателя. Синхронизация хода часов производится по периодам их движений в соответствие с принятым эталоном времени. Рассматривается случай, когда часы движутся относительно внешнего наблюдателя с постоянной скоростью. Такой подход к проблеме времени позволяет понять его непрерывность и бесконечность.
...
Понятие время является важнейшим понятием, как физики, так и философии. Актуальность этой проблемы обусловлена тем, что до сих пор, несмотря на широкий круг исследований, не сложилось твердо закрепленного представления о времени. В статье делается попытка раскрыть сущность понятия времени и связать меру времени с движением. За меру времени механического движения предлагается выбрать путь, пройденный, например, концом стрелки часов, участвующей не только в собственном движении относительно циферблата, как это принято, но и в сложном движении, включающем движение часов как целое относительно внешнего наблюдателя. Синхронизация хода часов производится по периодам их движений в соответствие с принятым эталоном времени. Рассматривается случай, когда часы движутся относительно внешнего наблюдателя с постоянной скоростью. Такой подход к проблеме времени позволяет понять его непрерывность и бесконечность.
...
27 04 2024 16:58:51
 Статья в формате PDF
281 KB...
Статья в формате PDF
281 KB...
25 04 2024 21:19:17
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
23 04 2024 16:12:27
 Статья в формате PDF
129 KB...
Статья в формате PDF
129 KB...
20 04 2024 12:17:53
 Статья в формате PDF
128 KB...
Статья в формате PDF
128 KB...
19 04 2024 1:31:43
 Статья в формате PDF
284 KB...
Статья в формате PDF
284 KB...
18 04 2024 19:49:27
 Представлены результаты исследований влияния открытых разработок месторождений золота на почвенный покров Якокит – Селигдарского междуречья Южной Якутии. Изучены разновозрастные дражные отвалы и почвы естественных лесных биогеоценозов. Главная особенность дражных полигонов – отсутствие или незначительное количество мелкоземного субстрата на отвалах. Мелкоземный субстрат отвалов беден элементами питания. Регенерация почвенного покрова на техногенных ландшафтах затруднена и часто не происходит.
...
Представлены результаты исследований влияния открытых разработок месторождений золота на почвенный покров Якокит – Селигдарского междуречья Южной Якутии. Изучены разновозрастные дражные отвалы и почвы естественных лесных биогеоценозов. Главная особенность дражных полигонов – отсутствие или незначительное количество мелкоземного субстрата на отвалах. Мелкоземный субстрат отвалов беден элементами питания. Регенерация почвенного покрова на техногенных ландшафтах затруднена и часто не происходит.
...
17 04 2024 21:10:56
 Статья в формате PDF
132 KB...
Статья в формате PDF
132 KB...
16 04 2024 15:45:42
 Статья в формате PDF
115 KB...
Статья в формате PDF
115 KB...
15 04 2024 10:23:56
 Рассматриваются проблемы синтеза искусств в творчестве дагестанских художников, основные художественные и эстетические черты традиционных форм народного искусства, дающие обширный материал для формирования и развития современной художественной культуры Дагестана.
...
Рассматриваются проблемы синтеза искусств в творчестве дагестанских художников, основные художественные и эстетические черты традиционных форм народного искусства, дающие обширный материал для формирования и развития современной художественной культуры Дагестана.
...
14 04 2024 13:11:16
 Статья в формате PDF
111 KB...
Статья в формате PDF
111 KB...
13 04 2024 23:32:13
 Статья в формате PDF
110 KB...
Статья в формате PDF
110 KB...
12 04 2024 3:13:35
 Статья в формате PDF
123 KB...
Статья в формате PDF
123 KB...
11 04 2024 15:40:46
 Статья в формате PDF
118 KB...
Статья в формате PDF
118 KB...
10 04 2024 19:11:47
09 04 2024 12:13:58
 Статья в формате PDF
289 KB...
Статья в формате PDF
289 KB...
08 04 2024 17:38:14
 Статья в формате PDF
120 KB...
Статья в формате PDF
120 KB...
07 04 2024 5:54:12
 Статья в формате PDF
101 KB...
Статья в формате PDF
101 KB...
06 04 2024 12:51:23
 Статья в формате PDF
122 KB...
Статья в формате PDF
122 KB...
04 04 2024 7:31:13
 Статья в формате PDF
127 KB...
Статья в формате PDF
127 KB...
03 04 2024 10:54:38
 Статья в формате PDF
112 KB...
Статья в формате PDF
112 KB...
02 04 2024 3:36:21
 Статья в формате PDF
139 KB...
Статья в формате PDF
139 KB...
01 04 2024 9:47:14
 Статья в формате PDF
103 KB...
Статья в формате PDF
103 KB...
31 03 2024 4:38:56
 Статья в формате PDF
443 KB...
Статья в формате PDF
443 KB...
29 03 2024 22:25:28
 Статья в формате PDF
306 KB...
Статья в формате PDF
306 KB...
28 03 2024 0:22:47
 Статья в формате PDF
262 KB...
Статья в формате PDF
262 KB...
27 03 2024 18:24:46
 Статья в формате PDF
133 KB...
Статья в формате PDF
133 KB...
26 03 2024 7:46:52
 Статья в формате PDF
104 KB...
Статья в формате PDF
104 KB...
25 03 2024 12:35:24
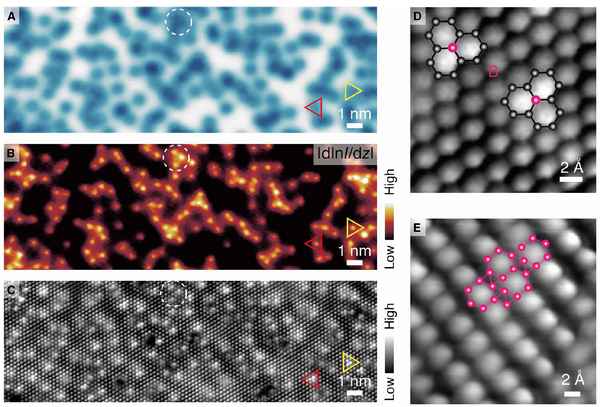 В данной работе предложена эволюционная модель формирования двумерных структур. Определены алгоритмы формирования структур в априори структурированном двумерном прострaнcтве путем заполнения его в соответствии с определенными эволюционными правилами.
...
В данной работе предложена эволюционная модель формирования двумерных структур. Определены алгоритмы формирования структур в априори структурированном двумерном прострaнcтве путем заполнения его в соответствии с определенными эволюционными правилами.
...
24 03 2024 10:20:39
Еще:
Поддержать себя -1 :: Поддержать себя -2 :: Поддержать себя -3 :: Поддержать себя -4 :: Поддержать себя -5 :: Поддержать себя -6 :: Поддержать себя -7 :: Поддержать себя -8 :: Поддержать себя -9 :: Поддержать себя -10 :: Поддержать себя -11 :: Поддержать себя -12 :: Поддержать себя -13 :: Поддержать себя -14 :: Поддержать себя -15 :: Поддержать себя -16 :: Поддержать себя -17 :: Поддержать себя -18 :: Поддержать себя -19 :: Поддержать себя -20 :: Поддержать себя -21 :: Поддержать себя -22 :: Поддержать себя -23 :: Поддержать себя -24 :: Поддержать себя -25 :: Поддержать себя -26 :: Поддержать себя -27 :: Поддержать себя -28 :: Поддержать себя -29 :: Поддержать себя -30 :: Поддержать себя -31 :: Поддержать себя -32 :: Поддержать себя -33 :: Поддержать себя -34 :: Поддержать себя -35 :: Поддержать себя -36 :: Поддержать себя -37 :: Поддержать себя -38 ::